GLP-1
GLP-1 : le pont entre
glucose, satiété et poids corporel
Dans le paysage actuel de la santé métabolique, le GLP-1 occupe une place centrale. Son importance croissante au sein de la communauté scientifique s’est manifestée par le développement de médicaments ciblant son récepteur. Cependant, au-delà de son application thérapeutique, une question plus profonde se pose : quel est le rôle du GLP-1 en tant que régulateur du métabolisme ?
Loin d’être simplement une « hormone de perte de poids », le peptide-1 de type glucagon (GLP-1) est un intégrateur métabolique qui relie la régulation du glucose, le contrôle de l’appétit et l’équilibre énergétique (1,2). Comprendre cet axe permet d’adopter une vision plus systémique du métabolisme.
Une hormone à fonction coordonnée
Le GLP-1 est une hormone incrétine produite par les cellules entéroendocrines L, principalement situées dans l’iléon et le côlon. Après sa sécrétion, il circule sous deux principales formes actives : GLP-1 (7–36) et GLP-1 (7–37), avec une demi‑vie courte en raison d’une dégradation rapide par l’enzyme DPP-IV (1).
Son action biologique dépend de sa liaison au récepteur du GLP-1 (GLP-1R), exprimé dans de nombreux tissus. L’activation de ce récepteur déclenche une signalisation intracellulaire dépendante de l’AMPc, qui (1,3) :
Stimule la sécrétion d’insuline dépendante du glucose
Inhibe la libération de glucagon
Préserve la masse fonctionnelle des cellules β pancréatiques
Améliore l’homéostasie glycémique postprandiale
Ce mécanisme positionne le GLP-1 comme un modulateur central du contrôle métabolique.
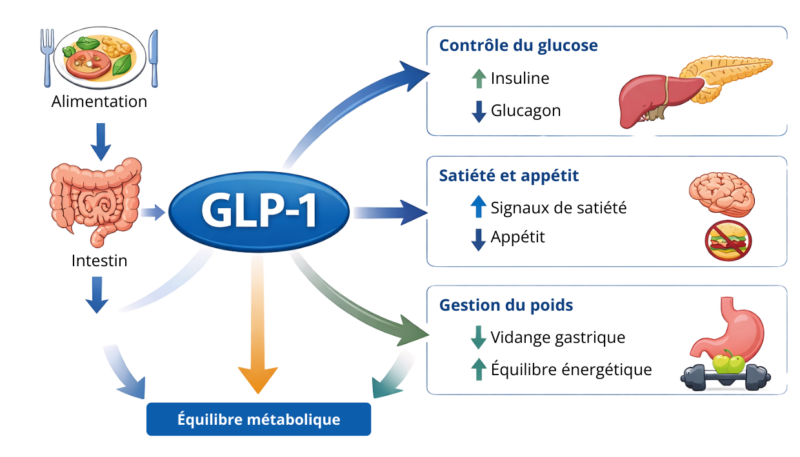
Schéma conceptuel basé sur (Wang et al., 2021 ; Domínguez-Avila et al., 2017 ; Derosa et al., 2025).
Point de départ :
Régulation du glucose
Au milieu de l’attention médiatique généralisée autour des analogues du GLP-1 tels que la sémaglutide (Ozempic) et le liraglutide (Saxenda), le discours public s’est largement concentré sur leurs effets sur la réduction du poids corporel. Cependant, cet accent a quelque peu éclipsé le rôle physiologique principal du GLP-1 : la régulation de la glycémie postprandiale, c’est-à-dire le contrôle de l’élévation de la glycémie après la prise alimentaire.
Une réponse glycémique postprandiale plus stable réduit à la fois la variabilité métabolique et l’hyperinsulinémie compensatoire, deux facteurs étroitement liés au développement progressif de la résistance à l’insuline et du diabète de type 2. Dans ce contexte, l’enjeu critique n’est pas seulement l’ampleur de l’élévation de la glycémie, mais l’efficacité avec laquelle l’organisme régule et s’adapte à cette augmentation (2,4,5).
Le diabète de type 2 n’apparaît pas brutalement ; il se développe progressivement à mesure que les tissus périphériques deviennent moins sensibles à l’insuline et que les cellules β pancréatiques subissent un déclin fonctionnel progressif. Lorsque ces processus convergent, le maintien de l’homéostasie glycémique devient compromis.
Dans ce cadre, le système des incrétines, et en particulier l’axe GLP-1/GLP-1R, revêt une importance physiologique majeure (1,3,6). Le GLP-1 stimule la sécrétion d’insuline dépendante du glucose, ce qui signifie que son action est amplifiée lorsque les concentrations de glucose augmentent après un repas, tout en inhibant simultanément la libération de glucagon. Cette réponse coordonnée permet un ajustement métabolique plus physiologique, contribuant à la préservation de la fonction des cellules β et à l’amélioration de la régulation métabolique globale (1,6).
En conséquence, les stratégies visant à optimiser le contrôle glycémique postprandial vont au-delà de la simple réduction du poids. Elles cherchent à améliorer la qualité et l’efficacité de la réponse métabolique à chaque repas, une approche aux implications plus larges pour la prévention et la prise en charge à long terme des troubles métaboliques (2,7,8).
GLP-1 et satiété :
la connexion intestin-cerveau
Au‑delà de son rôle dans le contrôle glycémique, le GLP-1 participe directement à la régulation de l’appétit. Cette hormone ralentit la vidange gastrique, prolongeant la sensation de satiété après les repas, et agit sur les neurones hypothalamiques exprimant le GLP-1R, modulant les signaux de satiété et réduisant la prise alimentaire (1).
Cet effet fait partie d’un système de rétroaction qui ajuste l’équilibre énergétique en fonction de l’état nutritionnel. Pendant le jeûne, les niveaux de ghréline augmentent et stimulent l’appétit ; après l’ingestion alimentaire, la sécrétion de GLP-1 augmente et contribue à réduire ce signal orexigène. L’interaction réciproque entre ces hormones reflète une régulation coordonnée de l’équilibre énergétique, démontrant que le GLP-1 répond non seulement au glucose, mais aussi à l’état métabolique global de l’organisme (1).
Microbiote et GLP-1
La fermentation des fibres alimentaires par le microbiote intestinal génère des acides gras à chaîne courte (AGCC), capables de moduler la sécrétion de GLP-1 (6). Cette relation renforce le rôle de l’intestin en tant qu’organe endocrinien clé dans la régulation métabolique et positionne l’interaction alimentation–microbiote–incrétine comme un axe pertinent dans la prévention cardiométabolique (8,9).
Régulation de la sécrétion de GLP-1 : un système multifactoriel
La sécrétion de GLP-1 répond à un système intégré de signaux neuronaux et nutritionnels. Après l’ingestion alimentaire, une phase précoce se produit, médiée par l’activation vagale et des mécanismes neuroendocriniens, suivie d’une seconde phase dépendant du contact direct des nutriments avec l’intestin (1). Dans cette dernière phase, le glucose, les acides gras, les AGCC dérivés du microbiote ainsi que les peptides ou acides aminés stimulent les cellules L intestinales via des récepteurs et transporteurs spécifiques (1,7).
Ce modèle confirme que le GLP-1 fonctionne comme un capteur métabolique de l’apport en nutriments.
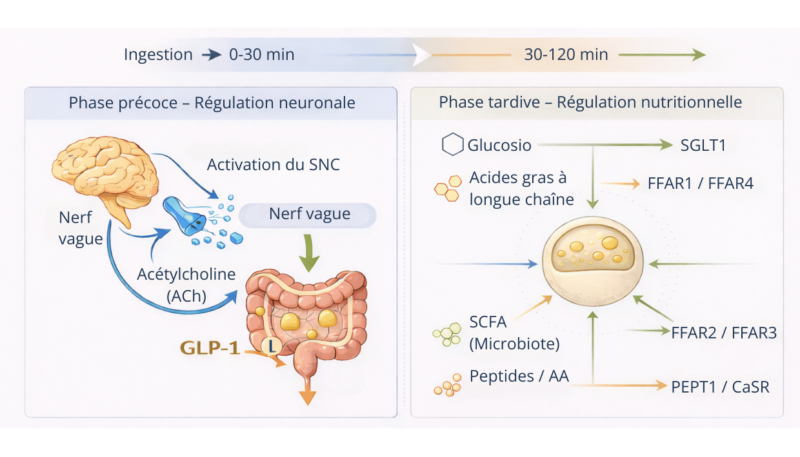
Adapté de (Wang et al., 2021 ; Domínguez-Avila et al., 2017 ; Iatcu et al., 2024).
Bien que son rôle principal soit le contrôle glycémique, le GLP-1 exerce également des effets sur d’autres tissus, avec des implications potentielles pour la fonction hépatique, la régulation cardiovasculaire et le métabolisme osseux (1). Dans l’ensemble, l’axe GLP-1/GLP-1R peut être considéré comme un nœud intégratif reliant l’intestin, le pancréas et le système nerveux central dans la régulation de l’équilibre métabolique.
Vous recherchez les bons ingrédients ?
Inscrivez-vous à notre newsletter…
…ou découvrez nos ingrédients dans le portefeuille de produits suivants !
Références
- Wang Y, Alkhalidy H, Liu D. The emerging role of polyphenols in the management of type 2 diabetes. Molecules. 2021;26(3):703.
- Derosa G, et al. Nutraceuticals and supplements in the management of prediabetes and diabetes: Mechanistic and clinical evidence. Nutrients. 2025;17(1):14.
- Domínguez Avila JA, et al. The antidiabetic mechanisms of polyphenols related to increased GLP-1 and insulin signaling. Molecules. 2017;22(6):903.
- Lown M, Fuller R, Lightowler H, Fraser A, Gallagher A. Mulberry-extract improves glucose tolerance and decreases insulin concentrations in normoglycaemic adults: A randomized double-blind placebo-controlled study. PLoS ONE. 2017;12(2):e0172239.
- Thondre PS, Lightowler H, Ahlstrom L. Mulberry leaf extract improves glycaemic response to sucrose in healthy subjects: A randomized, double-blind, placebo-controlled study. Nutrition & Metabolism. 2021;18:42.
- Abiola JO, et al. Potential role of phytochemicals as GLP-1 receptor agonists in diabetes. Pharmaceuticals. 2024;17(6):736.
- Iatcu OC, et al. Harnessing prebiotics to improve type 2 diabetes outcomes: Mechanisms and clinical relevance. Nutrients. 2024;16(20):3447.
- Venkatakrishnan K, et al. Functional foods and nutraceuticals in obesity and metabolic disorders. Food & Function. 2019;10:1240–1263.
- Cevallos-Fernández E, et al. Fermented plant-based foods and postbiotics for glycemic control: Mechanistic insights and clinical implications. Frontiers in Nutrition. 2026.






